ИММУНОКОРРЕКТОР ДЛЯ ЖИВОТНЫХ
РОНКОЛЕЙКИН®
РЕКОМБИНАНТНЫЙ ИНТЕРЛЕЙКИН-2
+7(911)916-02-00
vet@biotech.spb.ru
|
Рекомендации. Санкт-Петербург, 2004. 27 с. ПРИМЕНЕНИЕ ПРЕПАРАТА РОНКОЛЕЙКИН®
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Таблица 1 | ||||||
|
Клиническое состояние лошадей | ||||||
Клинические признаки |
Начало опыта |
Через 48 часов |
Через 21 день | |||
|
опыт |
контроль |
опыт |
контроль |
опыт |
контроль | |
Снижение аппетита |
нет |
нет |
незначительно в первые сутки |
нет |
нет |
нет |
Утомляемость, в "крестах": | ||||||
1 рысь 10 минут |
++ |
++ |
- |
++ |
+ |
++ |
| 2 рысь 10 минут |
+++ |
+++ |
- |
+++ |
- |
+++ |
| 3 рысь 10 минут |
+++ |
+++ |
+ |
+++ |
- |
+++ |
| Галоп 3 мин |
+++ |
+++ |
- |
+++ |
+ |
+++ |
| Ночной кашель, в "крестах" |
+++ |
+++ |
++ |
+++ |
+ |
+++ |
| Характер кашля, +/-: | ||||||
| Сухой отрывистый |
+ |
+ |
+ |
+ |
- |
+ |
| Сухой продолжительный |
+ |
+ |
- |
+ |
- |
+ |
| Влажный продолжительный |
- |
- |
+ |
- |
- |
- |
| Влажный отрывистый |
-/+ |
-/+ |
- |
- |
+ |
-/+ |
| Кашель во время нагрузки |
+ |
+ |
- |
+ |
- |
+ |
| Выделения из носа: | ||||||
| В покое |
-/+ |
-/+ |
+ |
-/+ |
- |
-/+ |
| Во время/после нагрузки |
+ |
+ |
+ |
-/+ |
- |
-/+ |
Результаты общего клинического обследования, таким образом, показали, что у лошадей, которым вводили Ронколейкин® уже после первой инъекции повысилась работоспособность: большинство из них несли обычную тренировочную нагрузку (без преодоления препятствий и продолжительного галопа) и не демонстрировали признаки утомления после первой рыси. В то же время лошади контрольной группы попрежнему показывали признаки утомляемости сразу после разминочной рыси. Следует отметить и изменение характера кашля у лошадей опытной группы. После первой инъекции Ронколейкина® значительно реже стал проявляться ночной кашель у животных, при этом из сухого он преобразовался во влажный и продолжительный. Такие признаки отмечались всего в течение 2-3 суток после однократного введения испытуемого препарата, затем у половины лошадей опытной группы кашель не проявлялся в течение всего времени эксперимента. Переход продолжительного влажного кашля у некоторых лошадей опытной группы в отрывистый, короткий, по-видимому, связан с отхождением остатков мокроты в течение длительного периода времени. Однако, мы считаем, это благоприятным признаком, тем более, что чаще всего он появлялся у лошадей во время нагрузки, в покое - нет.
Характерные изменения были обнаружены при аускультации: уже через 24 часа после первой инъекции Ронколейкина® в пораженных участках легких и трахее стали прослушиваться влажные хрипы. Уменьшение области поражения легочного поля мы стали отмечать после второго и третьего введения препарата. Стабильное клиническое улучшение мы наблюдали и по прошествии 3-х недель после окончания курса Ронколейкина® у 4 лошадей опытной группы. При этом отмечали нормализацию сердечной деятельности и отсутствие даже слабо выраженной экспираторной одышки в покое.
Следует отметить, что испытуемый препарат при подкожном введении дает, по-видимому, сильные болевые ощущения: все лошади опытной группы к окончанию введения препарата пытались уклониться от инъекции и затем в течение 1-2 минут продемонстрировали сильное беспокойство. Беспокойство выражалось в повышении двигательной активности, копании ногой, попытках лечь. Мы считаем, это кратковременной реакцией на болевые ощущения (раздражение?) в месте введения препарата, не требующей симптоматической терапии.
В то же время, у некоторых лошадей мы отмечали непродолжительное угнетение в первые сутки применения препарата. По-видимому, это связано с развитием эфемерной лихорадки на Ронколейкин® . Причем, интересен тот факт, что наибольший подъем температуры отмечался только после первой инъекции препарата, в дальнейшем такая реакция была выражена меньше. Результаты термометрии представлены на графике 1.
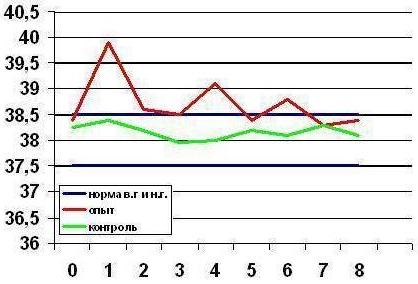
Рис.1. Ректальная температура лошадей опытной и контрольной групп
в динамике применения Ронколейкина® (1, 4, 6 - инъекции препарата)
Уместно также привести данные о формировании и характере очага асептического воспаления на месте инъекции Ронколейкина®. Мы принимали во внимание факт формирования припухлости на месте введения препарата, ее болезненность и время, через которое эти признаки самопроизвольно исчезали. Если отек в месте инъекции отсутствовал, мы учитывали уклонение лошади от пальпации участка шеи, где производилась инъекция (болезненность). Основные результаты клинических наблюдений приведены в таблице 2.
|
Таблица 2 | |||||||||
|
Характер асептического воспаления у лошадей опытной группы на месте введения Ронколейкина® | |||||||||
| Лошади | 1 инъекция |
2 инъекция |
3 инъекция | ||||||
| Наличие припух- лости |
Болезнен- ность в месте инъекции |
Исчезно- вение припух- лости |
Наличие припух- лости |
Болезнен- ность в месте инъекции |
Исчезно- вение припух- лости |
Наличие припух- лости |
Болезнен- ность в месте инъекции |
Исчезно- вение припух- лости | |
|
1. ж |
+ |
+ |
48 ч |
- |
- |
- |
+ |
+ |
24 ч |
| 2. ж |
+ |
+ |
24 ч |
+ |
+ |
12 ч |
+ |
+ |
24 ч |
| 3. ж |
- |
+ |
24 ч |
|
|
|
|
|
|
| 4. ж |
+ |
+ |
24 ч |
+ |
+ |
12 ч |
- |
+ |
6 |
| 5. к |
+ |
+ |
48 ч |
- |
- |
- |
- |
- |
- |
| 6. к |
- |
+ |
6 ч |
- |
- |
- |
- |
- |
- |
Из данных, приведенных в таблице 2, видно, что практически у всех лошадей отмечалась болезненная припухлость на месте введения препарата (кратковременная болезненность в момент введения препарата не учитывалась). Наиболее выраженным этот признак был у жеребцов - у них же, как показывают и другие клинические наблюдения, асептическое воспаление более продолжительное (до 48 часов) и наблюдается после каждой инъекции. В то же время у большинства лошадей очаг послеинъекционного воспаления формируется после первого введения препарата, а в дальнейшем может отсутствовать или быть слабо выраженным.
В дальнейшем, при использовании воды для инъекций вместо 0,9%-го раствора натрия хлорида в качестве разбавителя для ронколейкина мы перестали наблюдать выраженную отечность и болезненность на месте введения препарата.3.2. Влияние Ронколейкина® на сердечно-сосудистую систему
До начала эксперимента мы отметили, что со стороны сердечной деятельности у большинства больных лошадей наблюдаются функциональные нарушения, характерные для обструктивных заболеваний респираторных путей. Также у одной лошади в анамнезе (ЭКГ) были зафиксированы деструктивные изменения миокарда желудочков - есть катамнестические указания на перенесенный 2 года назад инфаркт миокарда. При обследовании данной лошади выявлены признаки хронической сердечной недостаточности: цианоз слизистых оболочек, быстрая утомляемость при минимальных нагрузках, отечность подгрудка и задних конечностей.
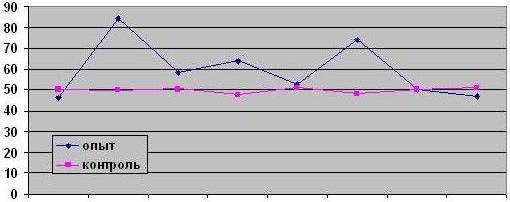
Ниже приведены данные о результатах клинического осмотра, мануальной пульсометрии и выборочной электрокардиографии животных опытной группы.
|
Таблица 3 | |||||||||
|
Электрокардиографические изменения у некоторых
лошадей опытной группы | |||||||||
|
Изменения на ЭКГ |
Количество выявленных
изменений, % от общего числа исследованных животных
| ||||||||
|
Начало опыта |
Через 12 часов после первой
инъекции |
Через 48 часов после первой
инъекции |
На 21-ые сутки после 3-й
инъекции | ||||||
| Тахикардия |
16,6 |
100,0 |
50,0 |
16,6 | |||||
| Укорочение интервалов PQ, ST |
0 |
33,3 |
0 |
0 | |||||
| Удлинение интервалов PQ, ST |
66,6 |
66,6 |
50,0 |
50,0 | |||||
|
Увеличение вольтажа зубцов Р, R, T |
16,6 |
33,3 |
33,3 |
33,3 | |||||
| Снижение вольтажа зубцов Р, R, T |
33,3 |
16,6 |
16,6 |
33,3 | |||||
| Смещение сегмента ST |
16,6 |
33,3 |
16,6 |
16,6 | |||||
| Экстрасистолия |
16,6 |
16,6 |
16,6 |
0 | |||||
Из приведенных в таблице 3 данных видно, что введение Ронколейкина® оказывает существенное влияние на величину и характер биоэлектрических потенциалов сердца. Результаты анализа ЭКГ животных опытной группы указывают на необходимость всестороннего и тщательного обследования животных с целью выявления деструктивных поражений миокарда до введения препарата. Принимая во внимание изменения ЭКГ в динамике применения Ронколейкина®, целесообразно рекомендовать применение медикаментозных средств, поддерживающих сердечную деятельность с началом введения препарата.
3.3. Влияние Ронколейкина® на гематологические показатели
Выявление основных изменений в гемограмме лошадей опытной и контрольной групп являются важным критерием эффективности испытуемого препарата. Несмотря на то, что в ветеринарной практике гематологическое исследование применяется гораздо реже, чем в гуманной медицине, картина крови при хронических обструктивных заболеваниях легких у лошадей является информативной. В течение проводимого нами эксперимента в зависимости от тяжести и продолжительности течения болезни мы обнаруживали как изменения, характерные для дыхательной недостаточности, так и неспецифические изменения, сопровождающие любые воспалительные процессы.В то же время наши исследования выявили положительное влияние Ронколейкина® на показатели крови лошадей опытной группы (табл.4 и рис.3).
Из данных, приведенных в таблице 4, видно, что до начала эксперимента у всех обследованных животных наблюдается картина эритроцитоза и гипергемоглобинемии - общее число эритроцитов, в среднем, и гемоглобина у большинства лошадей превышали физиологическую норму для данного вида животных. Такая картина может быть объяснена реализацией компенсаторных механизмов в условиях хронической дыхательной недостаточности. С этих же позиций мы рассматриваем и низкий уровень СОЭ, который в норме у лошадей обычно превышает 30 мм. На фоне высокого содержания клеток красной крови в начале опыта мы обнаруживали лейкопению у животных обеих групп. При этом следует отметить, что значительные изменения мы наблюдали при анализе лейкограммы. В начале опыта у лошадей двух групп был установлен нейтрофилез со сдвигом ядра влево. Причем, у некоторых лошадей сдвиг сопровождался дегенеративными изменениями в структурах нейтрофилов. Процентное содержание палочкоядерных нейтрофилов было высоким до начала эксперимента, но так и не достигало физиологических значений (у лошадей опытной группы) по завершении терапии Ронколейкином® .
При анализе гемограмм животных двух групп мы выявили достоверные различия, в основном после первой инъекции препарата. Так, через 48 часов после введения ронколейкина у лошадей опытной группы значительно снизилось содержание эритроцитов на фоне повышения числа клеток белой крови. При этом мы отметили повышение количества эозинофилов в периферической крови, не выходящее за рамки физиологической нормы, лимфоцитов и моноцитов. Хотя статистическая достоверность в отношении изменения числа моноцитов выявлена не была, мы считаем на общем фоне это благоприятным и учитываемым показателем. У лошадей контрольной группы колебания изученных показателей на всем протяжении эксперимента были незначительными, и в целом отражали картину хронической воспалительной реакции - нейтрофильный лейкоцитоз с ядерным сдвигом влево, лимфопения, и компенсированной дыхательной недостаточности - эритроцитоз.
Через 14 дней после завершения монотерапии Ронколейкином® у животных опытной группы число палочкоядерных нейтрофилов оставалось превышающим физиологическую норму, но в то же время возросло и количество лимфоцитов и моноцитов. Такую картину мы считаем благоприятным признаком, отражающим имунокорригирующую эффективность испытуемого препарата. Несмотря на незначительное снижение в течение всего времени эксперимента количество гемоглобина у опытных животных превышало физиологическую норму через 14 дней после окончания монотерапии Ронколейкином® . На фоне высокого же содержания эритроцитов (в пределах физиологической нормы) это свидетельствует о необходимом сохранении компенсаторных механизмов.
Особое внимание мы обратили на достоверное увеличение числа базофилов в динамике применения Ронколейкина® : к окончанию эксперимента этот показатель почти в 4 раза превышал физиологическую норму. Возможное объяснение этому - сенсибилизация организма лошадей к белковой структуре препарата. Однако, возникающая базофилия может иметь и другое происхождение, не связанное с применением Ронколейкина® - в контрольной группе этот показатель во все дни исследования был высоким, хотя и не достигал таких значений как в опытной.
Таким образом, по результатам гематологических исследований можно сделать вывод о преимущественно положительном корригирующем влиянии Ронколейкина® на гематологические показатели у лошадей, страдающих хроническими обструктивными заболеваниями легких. Подкожное введение Ронколейкина® трехкратно с интервалом 48 ч способствует повышению числа лимфоцитов и моноцитов в пределах физиологической нормы, снижает уровень палочкоядерных нейтрофилов в периферической крови, а также может обусловливать кратковременную базофилию в период терапии.
|
Таблица 4 | |||||||||
|
Влияние Ронколейкина® на
гематологические показатели лошадей при хронических обструктивных заболеваниях легких | |||||||||
| Показатели | Физиологическая норма |
Начало опыта |
Через 48 часов |
Через 14 дней | |||||
|
о |
к |
о |
к |
о |
к | ||||
| 1. Эритроциты, х1012/л |
6-9
х1012/л |
11,15±4,45 |
11,50 ± 3,45 |
9,81 ± 1, 87 |
11,52 ± 2,00 |
8,80 ± 1,05 |
11,75 ± 2,11 | ||
| 2. Лейкоциты, х 109/л |
8-12 х 109/л
|
9,20 ± 3,45 |
6,45 ± 1,00 |
10,7 ± 3,12 |
6,50 ± 1,45 |
9,96 ± 0,97 |
6,83 ± 2,45 | ||
| 3. СОЭ, мм/ч |
40-70 мм/ч |
18,16 ± 10,0 |
22,15 ± 4,57 |
23,5 ± 5,34 |
21,6 ± 3,45 |
25,7 ± 4,01 |
16,5 ± 3,72 | ||
| 4. Гемоглобин, г\л |
110-170 г/л |
142,33 ± 32,21 |
134,75 ± 16,37 |
130,3 ± 12,5 7 |
128,0 ± 22,7 |
127,5 ± 8,03 |
134,25 ± 10,7 | ||
| 5. Лейкограмма, % | |||||||||
| - Эозинофилы |
2-4 |
2,83 ± 0,44 |
2,75 ± 0,32 |
8,46 ±
0,97*1 |
1 2,11 ± 1,44 |
3,80 ± 0,44 |
4,63 ± 1,02 | ||
| - Базофилы |
0-1 |
1,41 ± 0,12 |
1,5 ± 0,05 |
9,00 ±
2,45*1 |
1 3,35 ± 0,50 |
3,40 ± 1,22 |
4,60 ± 1,33 | ||
| Нейтрофилы: | |||||||||
| - Миелоциты |
0 |
0,16 ± 0,01 |
0,5 ± 0,25 |
0,00 ± 0,00 |
0,75 ± 0,15 |
0,00 ± 0,00 |
0,50 ± 0,18 | ||
| -юные |
0 |
0,33 ± 0,15 |
0,75 ± 0,11 |
0,33 ± 0,15 |
1,00 ± 0, 50 |
1,39 ± 0,71 |
1,75 ± 0,50 | ||
| - палочкоядерные |
6-9 |
29,5 ± 2,44 |
31,25 ± 1,35 |
28, 1 ± 1,37 |
34,5 ± 0,87 |
15,8 ±
0,99*1 |
1 36,7 ± 3,75
| ||
| -сегментоядерные |
32-44 |
38,1 ± 3,01 |
39,5 ± 2,73 |
26,2 ± 2,71 |
37,9 ± 1,75 |
42,3 ± 3,44 |
34,3 ± 4,25 | ||
| Лимфоциты |
24-32 |
21,7 ± 2,17 |
22, 75 ± 3, 41 |
28,3 ±
0,75*1 |
21,8 ± 1,55 |
31,0 ±
2,02*1 |
1 17,52 ± 1,34
| ||
| Моноциты |
0-2 |
1,20 ± 0,33 |
0,00 ± 0,00 |
2,00 ±
0,04*1 |
0,00 ± 0,00
|
3,33 ±
0,11*1 |
1 0,00 ±
0,00 | ||
Примечание: Р < 0,05, рассчитано по отношению к предыдущему сроку исследования.

в динамике применения Ронколейкина®
4. МОНИТОРИНГ КЛИНИЧЕСКОГО БЛАГОПОЛУЧИЯ ЛОШАДЕЙ ОПЫТНОЙ ГРУППЫ
В течение клинического наблюдения за лошадьми, которым трехкратно инъецировался Ронколейкин®, мы обращали внимание на длительность сохранения эффекта клинического благополучия. Следует отметить, что период видимого клинического благополучия при монотерапии Ронколейкином® у разных лошадей был различным. У трех животных (50%) он сохраняется и на сегодняшний день, причем в эту группу входит жеребец с перенесенным инфарктом миокарда. У остальных лошадей ремиссия продолжалась 21 - 40 дней, затем признаки хронической респираторной обструкции постепенно возобновились. При этом (принимая во внимание и тех лошадей, которым ранее мы вводили Ронколейкин® с терапевтической целью, но в данном опыте они не участвовали) мы не отметили определенной зависимости от возраста животных, продолжительности и степени заболевания. Так, например, у 6-летнего и 1,5-летнего жеребцов ремиссия аллергической, вероятно, респираторной обструкции длилась 4 недели тогда как у возрастных лошадей (10-12 лет) она была более продолжительной - свыше 2 мес.
Наши дальнейшие наблюдения показали что сроки ремиссии можно продлевать путем ежемесячного (независимо от клинического благополучия лошади) подкожного 3-х кратного с интервалом 48 часов введения Ронколейкина®. Продолжительность ежемесячного введения ронколейкина составляет 3-6 месяцев (2-3 инъекции/месяц) в зависимости от длительности заболевания животного и его возраста.
5. КОМПЛЕКСНАЯ ТЕРАПИЯ ХРОНИЧЕСКОЙ БРОНХИАЛЬНОЙ ОБСТРУКЦИИ
Клинические наблюдения, проводившиеся нами более чем на 50 лошадях, страдающих обструктивными заболеваниями легких, позволили нам определить комплексный подход к терапии данной патологии с использованием Ронколейкина® .
Ниже приводится предлагаемая нами схема комплексной терапии с применением Ронколейкина® . Предлагаемая нами схема (рис. 4) имеет четкое научно-практическое обоснование, подтверждаемое рядом комплексных лабораторных и клинических мониторинговых исследований.
КОМПЛЕКСНАЯ ТЕРАПИЯ ХБО
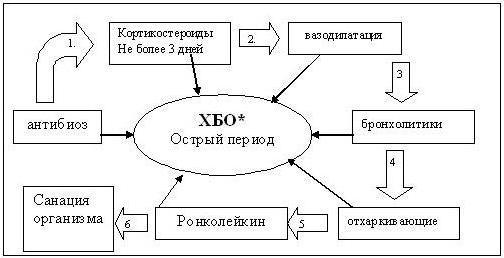
Пояснения к рис. 4:
1. Первый этап терапии основан на непродолжительном -
1-5 дней применении антибиотиков или фунгицидных средств. Как правило, мы
используем пролонгированные препараты пенициллинового ряда после
внутрикожной аллергопробы на лекарственную гиперчувствительность животного
(известно, что эти препараты иногда вызывают аллергическую
реакцию).
2. Одновременно с антибактериальной терапией
с момента острого бронхоспазма показано применение стероидных
противовоспалительных средств. Хорошо зарекомендовали себя в клинической
практике препараты преднизолона - преднизон, преднизолона сукцинат и их
аналоги. Препараты вводятся внутримышечно в дозе 0,25-1,0 мг/кг 3 дня
подряд, затем желательно снижение суточной дозы и их введение через день,
но, обычно, в целом, не более 5 инъекций. В этот же период проводят
медикаментозную поддержку сердечной деятельности с помощью препаратов,
рибоксин, кокарбоксилазы гидрохлорид, панангин и др.
3. Применение бронхолитических (эуфиллин, аналоги) препаратов
проводят с осторожностью, (так как ко многим из них у лошадей может
выработаться соматическая зависимость), сразу после курса
кортикостероидов. Целесообразно двух- трех-кратное внутримышечное введение
эуфиллина в дозе 4-10 мг/кг в зависимости от концентрации растворов.
4. После снятия, таким образом, острого бронхоспазма
можно применять бронходилататоры. В лечении лошадей хорошо зарекомендовал
себя вентипульмин в инъекционной форме и в виде сиропа. Препарат применяют
строго следуя инструкции, начиная с минимальной 0,8 мкг/кг дозы.
Недопустимо применение препарата до проведения антибактериальной и
противовоспалительной терапии, а также в период активной работы лошади.
5. В этот же период из расширенных расслабленных
бронхов целесообразно и наиболее эффективно удалять слизь и мокроту с
помощью отхаркивающих сиропов и микстур. Курс - 5-7 дней.
6. В целом последовательная терапия острого периода
занимает 10-14 дней. По окончании этого периода назначают непосредственно
иммуноориентированную терапию. С целью укрепления, в первую очередь,
клеточной и гуморальной активности вводят ронколейкин в дозе 1000 ед/кг на
0,9%-ном растворе натрия хлорида внутривенно капельно с интервалом 2 дня
всего 3 инъекции. Это завершающий и очень важный этап комплексной терапии
хронической бронхиальной обструкции лошадей. Если лечение проведено
принципиально правильно, то в дальнейшем Ронколейкин® применяют
в виде монотерапии только с целью пролонгации периода ремиссиии ежемесячно
2-3 подкожных инъекции в указанной дозе.
Предлагаемая нами схема медикаментозных воздействий, несомненно, должна сочетаться с определенными условиями содержания больных лошадей. Животным предоставляют гипоаллергенное кормление, длительный выпас в благоприятных условиях, легкую работу преимущественно на открытом грунте. В период обострения болезни лошадей освобождают от активной работы до клинического выздоровления.
ЗАКЛЮЧЕНИЕ
- Препарат Ронколейкин® оказывает корригирующее влияние на картину крови лошадей, страдающих хронической респираторной обструкцией:
- способствует повышению числа лимфоцитов и моноцитов в пределах физиологической нормы;
- снижает уровень палочкоядерных нейтрофилов в периферической крови;
- может обусловливать кратковременную базофилию в период терапии. - Ронколейкин® при подкожном введении в дозе 500 тыс Ед./гол (m=450-500кг) курсом 3 инъекции с интервалом 48 часов способствует снижению обструктивных воспалительных явлений в респираторных путях лошадей и повышению работоспособности животных.
- Продолжительность ремиссии после вышеуказанного курса монотерапии ронколейкином у больных респираторной обструкцией лошадей составляет 21 - 60 дней.
- При подкожном введении лошадям Ронколейкин® в указанных дозах и способах разведения (0,9% раствором натрия хлорида) вызывает кратковременную (2-3 мин) болезненность и образование припухлости, исчезающей в течение 12 - 48 часов.
- Ронколейкин® в указанных дозах и способах введения у лошадей способствует развитию эфемерной лихорадки.
- В течение 2 -24 часов после введения под кожу Ронколейкин® обусловливает синусовую тахикардию и кратковременную функциональную аритмию. У лошадей, страдающих органическими поражениями миокарда и клапанного аппарата сердца препарат может вызвать отсроченную соматическую реакцию.
- Ронколейкин® может использоваться в качестве иммунокорригирующего средства лошадям при хронических обструктивных заболеваниях легких в качестве комплексной или монотерапии.
СПИСОК ЛИТЕРАТУРЫ
1. Кондрахин Н.П. и др. Клиническая лабораторная диагностика в
ветеринарии: Справочное изд. под ред. И.П.Кондрахина, И.В.Курилова,
А.Г.Малахова и др. М.: Агропромиздат, 1985. 287 с.
2. Романова О.В.,
Лютинский С.И. Аллергические и аутоиммунные болезни лошадей. Патогенез.
Симптомы. Лечение. СПб.: Ясный Свет, 2002. 108 с.
3. Ронколейкин®
- рекомбинантный интерлейкин-2 человека. Под ред. В.К.Козлова. СПб.,
2001. 48 с.
4. Ammann. V.J., Vrins A.A., and Lavoie J.P. Effects of
inhaled beclomethasone dipropionate on respiratory function in horses with
chronic pulmonary disease (CORD). Equine Veterinary Journal. 1998. 30(2).
P. 152-157.
5. Beech J. Chronic lower airway inflammation, chronic
obstructive pulmonary disease; diagnosis, treatment and management.
Ippologia. 1997. 8(4). P. 5-14.
6. Couetil L.L., Rosenthal F.S., de
Nicola D.V. et al. Clinical signs, evaluation of bronchoalveolar lavage
fluid, and assessment of pulmonary function in horses with inflammatory
respiratory disease. American Journal of Veterinary Research. 2001. 62(4).
P. 538-546.
7. Derksen F. et al. Chronic obstructive pulmonary
disease: equine roundtable discussion. Equine Practice. 1991. 13 (5). P.
28-32.
8. Ferro E. et al. Chronic obstructive pulmonary disease in the
horse (CORD). Ippologia. 1993. 4(2). P. 71-78.
9. Ferro E. et al.
Therapy of chronic obstructive pulmonary disease(CORD) in the horse.
Ippologia. 1993. 4(3). P. 56-67.
10. Hoffman A.M. et al. Management of
severe obstructive pulmonary disease with inhaled bronchodilator treatment
in a horse. Canadian veterinary Journal. 1993. 34(8). P. 493-495.
11.
Lekeux P., Art T., and Roberts C. Control of chronic obstructive pulmonary
disease in the horse. British Veterinary Journal. 1996. 152(4). P.
365-367.
12. Robinson N.E. et a. The pathogenesis of chronic
obstructive pulmonary disease of horse. British Veterinary Journal.- 1996.
152(3). P. 283-286.
13. Sellnow L. Chronic obstructive pulmonary
disease. The Horse: Your Guide to Equine Health Care.- 1997. 14(11). P.
57-67.
14. Viel L. et al. Therapeutic efficacy of inhaled
fluticonasone propionate in horses with chronic obstructive pulmonary
disease. Proceedings of the Annual Convention of the American Association
of Equine Practitioners. 1999. (45). P. 306-307.
